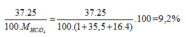Trong tự nhiên clo có hai đồng vị bền là 35Cl và 37Cl trong đó 35Cl chiếm 75,77% số nguyên tử. Phần trăm khối lượng 37Cl trong HClOn là 13,09%. Giá trị của n là
A.1
B.2
C.3
D.4
Câu 30: Trong tự nhiên clo có 2 đồng vị bền là 35cl và 37cl trong đó 35cl chiếm 75.77% số nguyên tử. Phần trăm khối lượng 37Cl trong đó HCLOn là 13,09% giá trị của n là ?
%35Cl = 100 - 24,23 = 75,77%=> MCl = 37 x 0,2423 + 35 x 0,7577 = 35,4846 (g/mol)
=> %37Cl trong CuCl2 = \(\dfrac{0,2423.37}{64+35,4846.2}\).100% = 6,64%
Trong tự nhiên clo có hai đồng vị bền là 35Cl và 37Cl. Nguyên tử khối trung bình của Cl là 35,4886. Thành phần % khối lượng của 35Cl trong PClx là 18,66% (P=31). Tìm giá trị của x.
Câu 11: Trong tự nhiên clo có hai đồng vị bền là 35Cl và 37Cl. Nguyên tử khối trung bình của Cl là 35,4886. Thành phần % khối lượng của 35Cl trong PClx là 18,66% (P=31). Tìm giá trị của x
Giả sử % số nguyên tử của đồng vị 37Cl là x%, suy ra % số nguyên tử đồng vị 35Cl là (100-x)%
Nguyên tử khối trung bình của Clo được tính theo công thức:
ACl¯=37x+35(100−x)\100=35,5
Giải phương trình trên được x= 25%
=>35Cl=100-25=75%
Vậy % khối lượng của 35Cl trong KClO3 là:
%m37Cl= 0,75.35.100%\31+33,5.x=18,66%
=>x=3
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17).
Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H = 1, O = 16):
A. 8,92%
B. 8,43%
C. 8,56%
D. 8,79%
Đáp án A
• %35Cl = 100% - 24,23% = 75,77%
→ MCl = 37 x 0,2423 + 35 x 0,7577 = 35,4846.
→ Thành phần % của 37Cl trong HClO4 là
![]()
Nguyên tố Clo có hai đồng vị bền là: 35Cl(75,77%) và 37Cl(24,23%)
a, Tính số nguyên tử của từng đồng vị trong 8,96l khí Clo(đktc) và nguyên tử khối trung bình của Clo
b, Tính phần trăm về khối lượng của 35Clo có trong FeCl3. Cho Fe=56
Áp dụng công thức tính nguyên tử khối trung bình:
Trong đó đồng vị A có x% số nguyên tử, đồng vị B có y% số nguyên tử.
Vậy nguyên tử khối trung bình của nguyên tố clo bằng:
Trong tự nhiên Clo có 2 đồng vị 35Cl và 37Cl. Nguyên tử khối trung bình của Clo là 35,5. Phần trăm về khối lượng của 35Cl trong HClO là
A.50,00%.
B.48,67%.
C.51,23%.
D.55,20%.
Đáp án A.
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
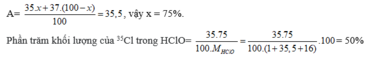
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35Cl và 37Cl. Phần trăm về khối lượng của ![]() ) là giá trị nào sau đây
) là giá trị nào sau đây
A. 9,40%
B. 8,95%
C. 9,67%
D. 9,20%
Đáp án D
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có
A = ![]() = 35,5, vậy x = 75%
= 35,5, vậy x = 75%
Phần trăm khối lượng của 37Cl trong HClO4 = 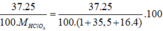 = 9,2%
= 9,2%
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35Cl và 37Cl. Phần trăm về khối lượng của C 17 37 l chứa trong HClO4 (với hiđro là đồng vị H 1 1 , oxi là đồng vị O 8 16 ) là giá trị nào sau đây
A. 9,40%.
B. 8,95%.
C. 9,67%.
D. 9,20%.
Đáp án D.
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=